Milada Teplá
KUDCH, PřF UK v Praze
email: milada.tepla@natur.cuni.cz
Biochemie - základní kapitoly
Buňka - úvod
Nukleové kyseliny a proteosyntéza
Přírodní látky
Trávení
Metabolismus
- Základní pojmy
- Metabolismus sacharidů
- Metabolismus triacylglycerolů
- Metabolismus bílkovin
- Citrátový cyklus
- Vztahy mezi metabolismy
- Lokalizace pochodů v buňce
- Dýchací řetězec
- Fotosyntéza
- Photosynthesis
- Electron Transport Chain
- Výukové materiály
Další informace
Fotosyntéza - úvod
Pro běžnou výuku ve vyšších ročnících gymnázia / střední školy doporučuji následující materiály (videa a studijní text):
Videa:
Studíjní text:
- kap. 1.: Úvod,
- kap. 2.1: Jakou funkci mají fotosyntetické pigmenty ve fotosyntéze?
- kap. 2.4: Jak se tvoří ATP?
- kap. 2.5: Primární děj fotosyntézy – schéma
- kap. 3.1: K čemu dochází v Calvinově cyklu a kde reakce Calvinova cyklu probíhají?
Nebo též článek dostupný v časopise Přírodovědci: Tajemství fotosyntézy
Fotosyntéza - pro pokročilé
Pro výuku určenou do chemického/biologického semináře střední školy, vysokoškolskou výuku jsou určené náasledující materiály:
Videa:
Celý playlist Fotosyntéza zde: https://www.youtube.com/watch?v=lP17DVasqHY&list=PLLvU1fRuTbvRt3twif_A75v_WqQsTIU6Y
Studijní text
1. Úvod
1.1. Lokalizace fotosyntetických dějů v buňce, struktura chloroplastu
2. Primární fáze fotosyntézy
2.1. Jakou funkci mají fotosyntetické pigmenty ve fotosyntéze?
2.2. Jak molekula chlorofylu v reakčním centru zachycuje světelnou energii?
2.3. Jak se elektron z reakčního centra fotosystému II přenese na NADP-reduktasu?
2.4. Jak se tvoří ATP?
2.5. Primární děj fotosyntézy – schéma
2.6. Jak se mění redoxní potenciál v závislosti na průběhu fotosyntézy?
2.7. Cyklický tok elektronů
3. Sekundární fáze fotosyntézy
3.1. K čemu dochází v Calvinově cyklu a kde reakce Calvinova cyklu probíhají?
3.2. Fotorespirace a C4 rostliny
4. Kvíz fotosyntéza
5. Seznam zkratek
6. Použitá literatura
1. Úvod
Fotosyntéza je jeden z nejdůležitějších dějů v přírodě, V průběhu fotosyntézy dochází k zachycení sluneční energie (fotonů) a k následné syntéze organických látek (sacharidy, mastné kyseliny a prekurzory aminokyselin) z oxidu uhličitého a vody. Mezi organismy mající schopnost provádět fotosyntézu patří vyšší rostliny, zelené a hnědé řasy, jednobuněčné sinice, zelené a purpurové bakterie. Reakce probíhající během fotosyntézy se dají rozdělit do dvou základních dějů: primární děj (přenos elektronů a protonů) a sekundární děj (fixace uhlíku – Calvinův cyklus).
Sumární reakce fotosyntézy: 6 CO2 + 12 H2O → C6H12O6 + 6 O2 + 6 H2O
1.1. Lokalizace fotosyntetických dějů v buňce, struktura chloroplastu
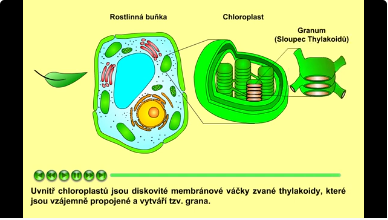
Celý proces fotosyntézy je u eukaryotních organismů lokalizován v chloroplastech. Uvnitř chloroplastů jsou diskovité membránové váčky zvané thylakoidy, které jsou vzájemně propojené a vytváří tzv. grana.
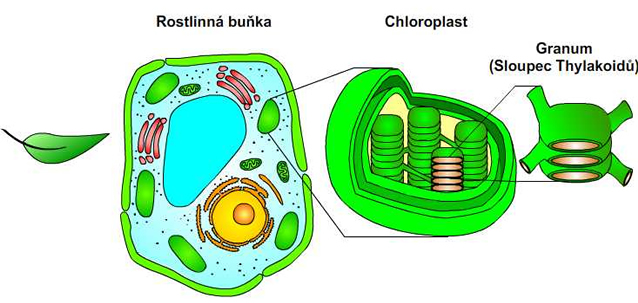
Obr. 1: Průřez listem. Viz též animace / video / youtube: https://youtu.be/u6-SIU7vm_w.
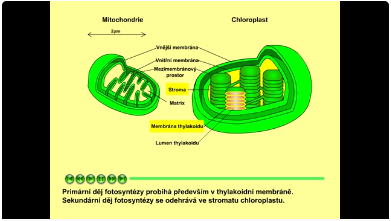
Chloroplasty jsou organely velmi podobné mitochondriím. Mají tři typy membrán: vnější membránu, vnitřní membránu a membránu thylakoidů. Membrány určují tři oddělené prostory: mezimembránový prostor, stroma a lumen thylakoidů. Chloroplast patří mezi semiautonomní organely, tzn., že obsahuje svoji vlastní DNA. Primární děj fotosyntézy probíhá především v thylakoidní membráně. Sekundární děj fotosyntézy se odehrává ve stromatu chloroplastu.
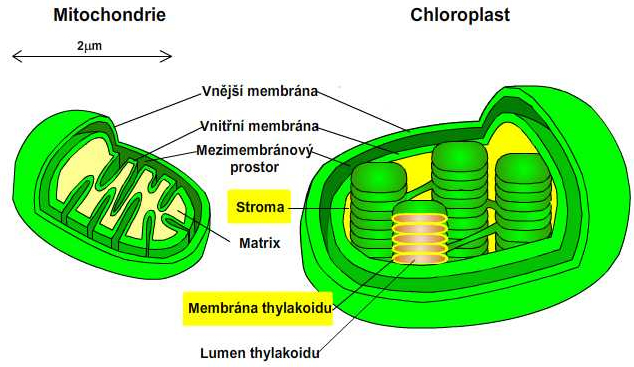
Obr. 2: Složení mitochondrie a chloroplastu. Viz též animace / video / youtube: https://youtu.be/ufZ1KjptURY.
2. Primární fáze fotosyntézy
2.1. Jakou funkci mají fotosyntetické pigmenty ve fotosyntéze?
Fotosyntéza je pochod poháněný světlem (energií fotonu). Chloroplasty obsahují rostlinné pigmenty, které mají mnoho konjugovaných dvojných vazeb. Takovéto molekuly silně pohlcují viditelné světlo. Hlavní rostlinný pigment je chlorofyl. Chlorofyly lze řadit mezi cyklické tetrapyroly (porfyriny) s komplexně navázaným hořečnatým iontem. Na pyrolové jádro je vázán zbytek alkoholu fytolu (C20), který jim uděluje hydrofobní povahu (viz obr. „Vzorec chlorofylu a, b“).
Kromě chlorofylů, rostliny obsahují i jiné pigmenty (např. karoteny a xanthofyly). Karoteny (např. β-karoten) jsou nenasycené alifatické uhlovodíky o sumarním vzorci C40Hx. Xanthofyly (např. lutein) jsou deriváty β-karotenu obsahující v molekule kyslíkaté zbytky (viz obr. „Vzorec karotenu a luteinu“).
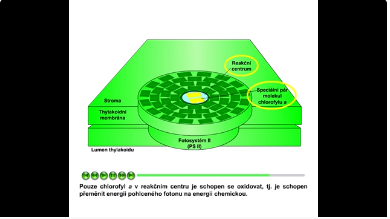
Primární fotosyntetická reakce probíhá ve fotosyntetických reakčních centrech, které jsou lokalizovány v thylakoidní membráně. Reakční centrum je součástí fotosystému I i II a obsahuje speciální pár molekul chlorofylu a. Pouze chlorofyl a v reakčním centru je schopen se oxidovat, tj. je schopen přeměnit energii pohlceného fotonu na energii chemickou. Ostatní pigmenty fungují jako světlosběrné antény, tj. předávají si energii pohlceného fotonu z jedné molekuly antenního pigmentu na druhou, až nakonec energie pohlceného fotonu dospěje do fotosyntetického reakčního centra, kde dojde k oxidaci molekuly chlorofylu a. Tyto světlosběrné pigmenty (cholrofyl a a b, karoteny a lutein) jsou součástí světlosběrného komplexu.
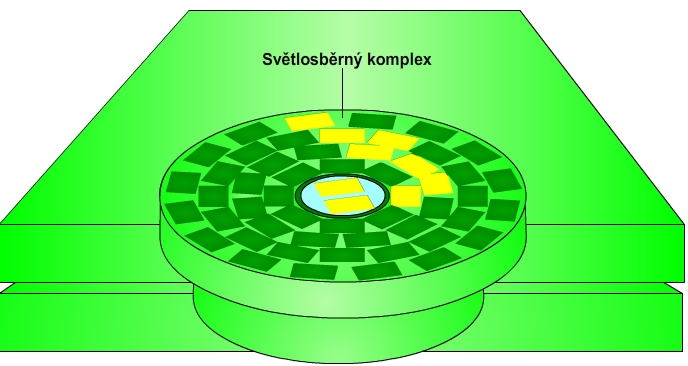
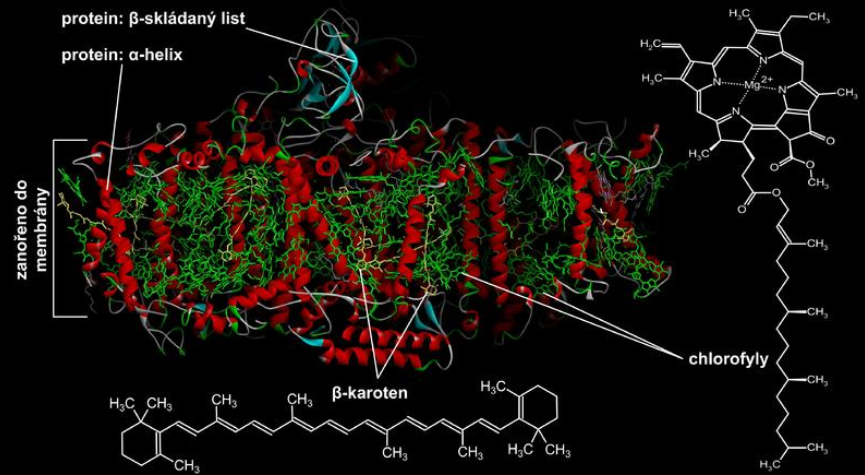
Obr. 3 a 4: Světlosběrný komplex. Na obrázku níže je znázorněna struktura fotosystému I Hrachu setého (Pisum sativum). Zeleně jsou vyznačeny molekuly chlorofylů, žlutě molekuly β-karotenu (pigment patřící do skupiny karotenoidů). Viz též animace / video / youtube: https://youtu.be/tqYNNxtILFQ.
2.2. Jak molekula chlorofylu v reakčním centru zachycuje světelnou energii?
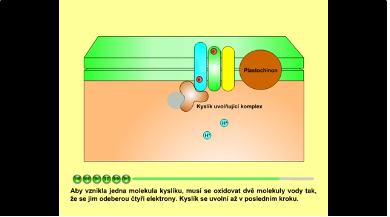
Reakční centrum fotosystému je proteinový komplex, který v sobě váže speciální pár molekul chlorofylu a. Chlorofyl a v reakčním centru PS II se označuje P680, podle vlnové délky maxima své absorpce. Po dopadu fotonu dojde k vyzáření elektronu, který je předán akceptoru. Vzniká kladně nabitá molekula chlorofylu, která je velmi silným oxidačním činidlem. Kladně nabitá molekula chlorofylu ihned přebírá elektron od donoru a vrací se do svého základního stavu. Donor elektronu se regeneruje elektronem vzniklým fotolýzou vody. Kyslík uvolňující komplex naváže dvě molekuly vody a usnadňuje vznik kyslíku tím, že postupně odjímá elektrony a protony. Protony se uvolňují do lumen thylakoidu. Elektron z akceptoru (= feofytin) je přenášen na plastochinon. Aby vznikla jedna molekula kyslíku, musí se oxidovat dvě molekuly vody tak, že se jim odeberou čtyři elektrony. Kyslík se uvolní až v posledním kroku. Kyslík se uvolňuje do ovzduší.
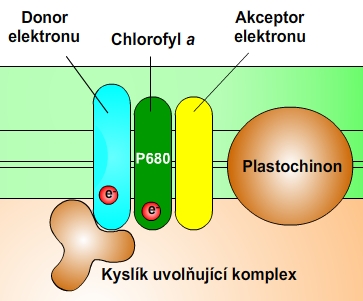
Obr. 5: Reakční centrum fotosystému II. Viz též animace / video / youtube: https://youtu.be/Yh2fzlwYoq8.
2.3. Jak se elektron z reakčního centra fotosystému II přenese na NADP-reduktasu?
Oxygenní fotosyntéza probíhá na třech komplexech (cytochrom b6-f komplex, PS I and II), které prostupují thylakoidní membránou. Mezi těmito komplexy přenášejí elektrony pohyblivé přenašeče: plastochinony (pQ) a plastocyanin (pC).
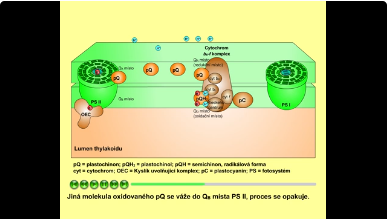
Elektron z feofytinu je přenášen na molekulu plastochinonu (pQ), která je pevně vázána na PS II v QA místě. Plastochinon v QA místě se chová jako jednoelektronový akceptor. Elektron je přenášen na další molekulu pQ, která je slabě vázána na PS II v QB místě. Plastochinon v QB místě se chová jako dvouelektronový akceptor. Úplná redukce pQ na plastochinol (pQH2) vyžaduje vazbu dvou elektronů a dvou protonů. Zredukovaná molekula pQH2 se uvolní z PS II a pohybuje se thylakoidní membránou až do oxidačního místa (QO místo) cytochrom b6-f komplexu. Jiná molekula oxidovaného pQ se váže do QB místa PS II, proces se opakuje. Molekula pQH2 v QO místě je oxidována cytochrom b6-f komplexem. Jeden z elektronů přechází na Rieskeho centrum (Fe2S2), druhý elektron přechází na cytochrom bL. Elektron z Rieskeho centra přechází na cytochrom f, z něhož přechází na malý protein zvaný plastocyanin (pC). Plastocyanin (pC) předává elektrony z cytochromu f na fotosystém I (PS I). Elektron z cytochromu bL je přenesen na cytochrom bH a následně na jinou oxidovanou molekulu pQ, která je vázána v redukčním místě (QR místo). Oxidovaná molekula pQ je uvolněna z QO místa a je nahrazena redukovanou molekulou pQH2. Další molekula oxidovaného pQ se váže do QB místa PS II. Redukovaná molekula pQH2 je oxidována cytochrom b6-f komplexem v oxidačním místě (QO místo). pQH2 je následně uvolněna z QR místa a váže se do QO místa. Jiná molekula oxidovaného pQ se váže do redukčního místa (QR místa). Procesy se opakují. Při tomto přenosu se na jeden elektron, který projde cytochrom b6-f komplexem, zároveň přenesou dva protony ze stromatu do lumen thylakoidu. Tento mechanismus se nazývá "Q-cyklus".
Protony a elektrony jsou přenášeny skrze oxidačně-redukční smyčku zvanou Q-cyklus.
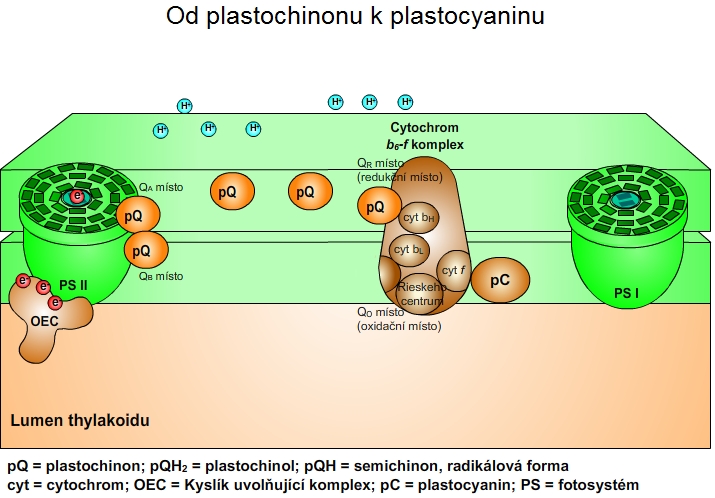
Obr. 6: Od plastochinonu k plastocyaninu - přenos elektronů mezi PS II a PS I.
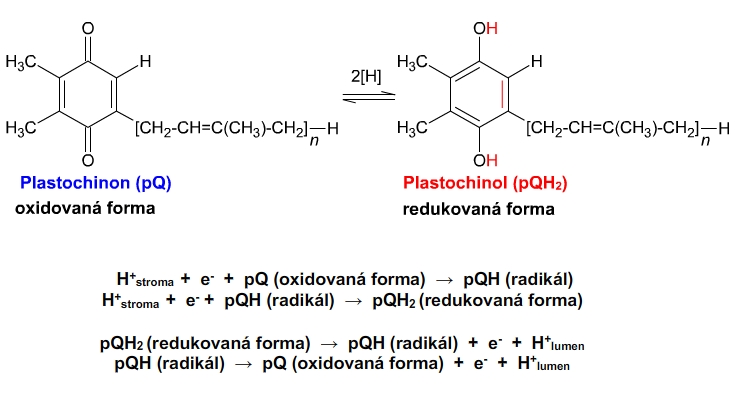
Obr. 7: Q-cyklus.
Od plastochinonu k plastocyaninu: Viz též animace / video / youtube: https://youtu.be/zC6_Y0kO-hk.
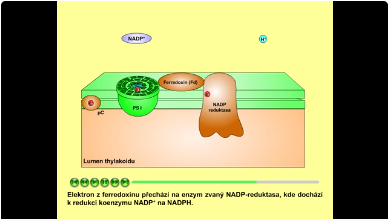
Fotony v PS I pohlcuje molekula chlorofylu a s absorpčním maximem při vlnové délce 700 nm (P700). Uvolněná energie je využita pro excitaci elektronu z molekuly chlorofylu a. Excitovaný elektron přebírá akceptor fotosystému I, ze kterého přechází na ferredoxin (Fd). Oxidovaná molekula chlorofylu přijímá elektron z plastocyaninu (pC). Plastocyanin přebírá elektron z cytochrom b6-f komplexu a vrací se do svého původního stavu. Elektron z ferredoxinu přechází na enzym zvaný NADP-reduktasa, kde dochází k redukci koenzymu NADP+ na NADPH
NADP+ + H+ + 2e- → NADPH (nikotinamidadenindinukleotidfosfát)
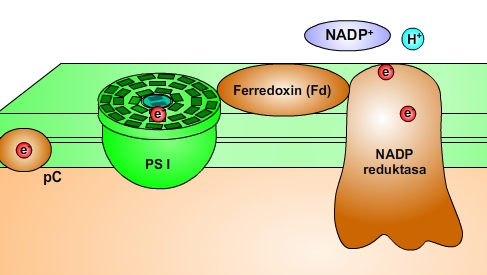
Obr. 8: Fotosystem I a NADP-reduktasa.Viz též animace / video / youtube: https://youtu.be/nqCqKeGL7dQ.
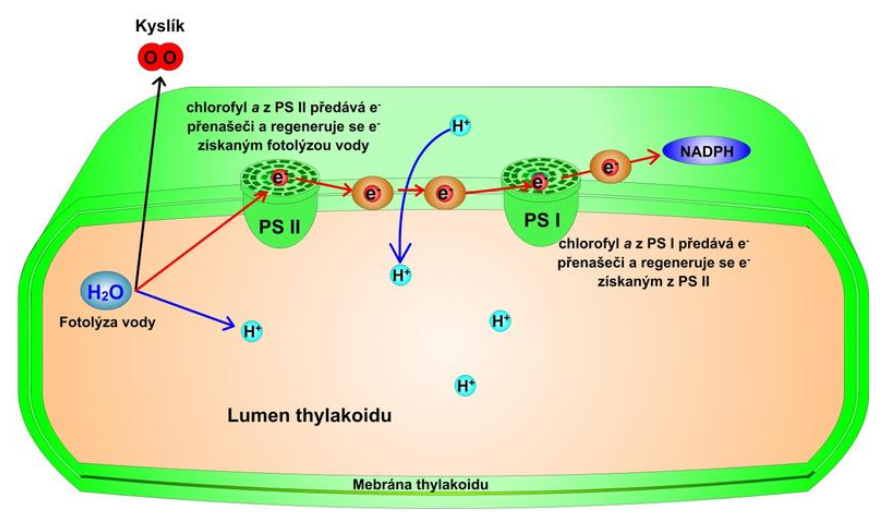
Obr. 9: Zjednodušené schéma přenosu elektronu na NADPH.
2.4. Jak se tvoří ATP?
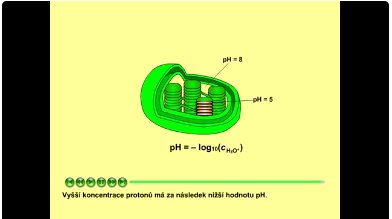
V průběhu fotosyntézy se vytváří elektrochemický protonový gradient. Prvním procesem, který přispívá ke vzniku protonového gradientu, je fotolýza vody. Druhým procesem, který přispívá ke vzniku protonového gradientu, je přenos protonů ze stromatu do lumen prostřednictvím plastochinonu (na každý přenesený elektron jsou přeneseny přibližně 2 protony). Třetím procesem, který přispívá ke vzniku protonového gradientu, je redukce NADP+ na NADPH. Při této reakci jsou spotřebovány dva protony. Tyto tři procesy vytvářejí elektrochemický protonový gradient (koncentrace protonů je v lumen daleko vyšší než ve stromatu). Vyšší koncentrace protonů má za následek nižší hodnotu pH (pHlumen = 5, pHstroma = 8).
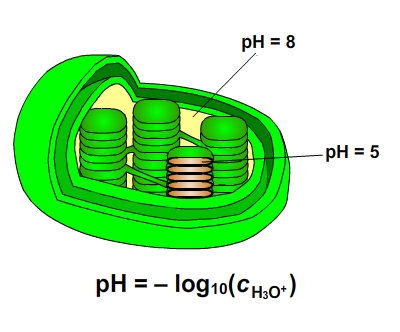
Obr. 10: pH rozdíly. Viz též animace / video / youtube: https://youtu.be/42c3ghikzNE.
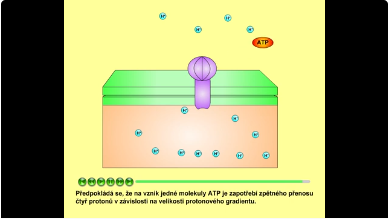
Energie uložená v rozdílu koncentrací protonů na obou stranách membrány se využívá k syntéze ATP (adenosintrifosfát) prostřednictvím ATP-synthasy. Při přechodu protonů zpět do stromatu vzniká energie, která pohání syntézu ATP (adenosintrifosfát) z ADP (adenosindifosfát) a anorganického fosfátu P. Tato syntéza ATP se nazývá fotofosforylace. Předpokládá se, že na vznik jedné molekuly ATP je zapotřebí zpětného přenosu čtyř protonů v závislosti na velikosti protonového gradientu. ATP přechází do Calvinova cyklu, kde se zpět rozkládá na ADP a anorganický fosfát, přičemž se uvolňuje energie.
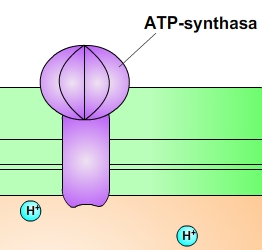
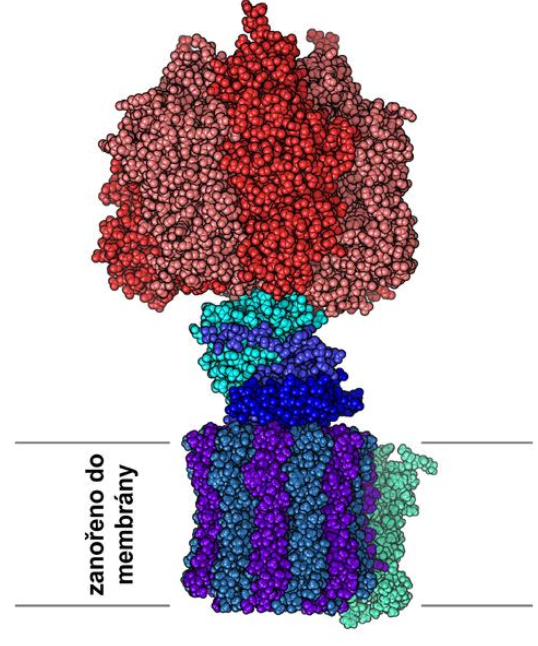
Obr. 11 a 12: ATP-synthasa. Na obrázku níže je struktura ATP synthasy (Zdroj Wikimedia Commons, autor Alex.X - enWiki (PDB.org for coordinate), CC BY-SA 3.0). Viz též animace / video / youtube: https://youtu.be/lzEW_k9_BZ0.
2.5. Primární děj fotosyntézy – schéma
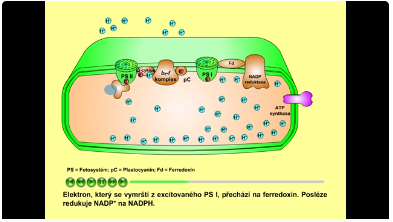
U rostlin dochází k fotochemickým reakcím ve dvou reakčních center patřících PS I a PS II, která pracují v sérii. Z excitovaného PS II se vymrští elektron, který prochází řadou přenašečů až na PS I. Elektron, který se vymrští z excitovaného PS I, přechází na ferredoxin. Posléze redukuje NADP+ na NADPH. Energie uložená v rozdílu koncentrací protonů na obou stranách membrány se využívá k syntéze ATP prostřednictvím ATP-synthasy. PS II obsahuje kyslík uvolňující komplex, který oxiduje 2H2O na 4H+ a kyslík, který se uvolní až po odebrání všech čtyř elektronů. Produkty (NADPH a ATP) přecházejí do Calvinova cyklu, kyslík se uvolňuje do ovzduší.
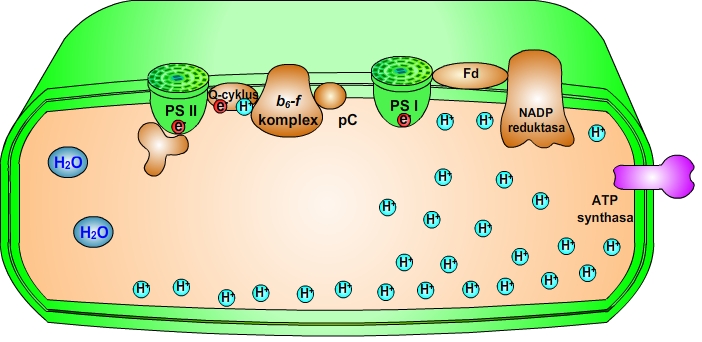
Obr. 13: Primární fáze fotosyntézy (PS- fotosystém, Fd - ferredoxin, pC - plastocyanin). Viz též animace / video / youtube: https://youtu.be/IDp3zRBP5PM.

Obr. 9: Zjednodušené schéma přenosu elektronu na NADPH.
2.6. Jak se mění redoxní potenciál v závislosti na průběhu fotosyntézy?
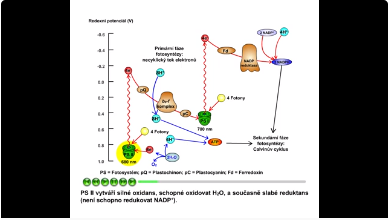
PS II vytváří silné oxidační činidlo, schopné oxidovat H2O, a současně slabé redukční činidlo (není schopno redukovat NADP+). PS I vytváří slabé oxidační činidlo (není schopné oxidovat vodu) a současně silné redukční činidlo, které je již schopno redukovat NADP+. Slabé redukční činidlo (PS II) je schopno redukovat slabé oxidační činidlo (PS I). Aby se mohl uskutečnit fotosyntetický přenos elektronů z H2O na NADP+, musí fungovat společně oba fotosystémy).
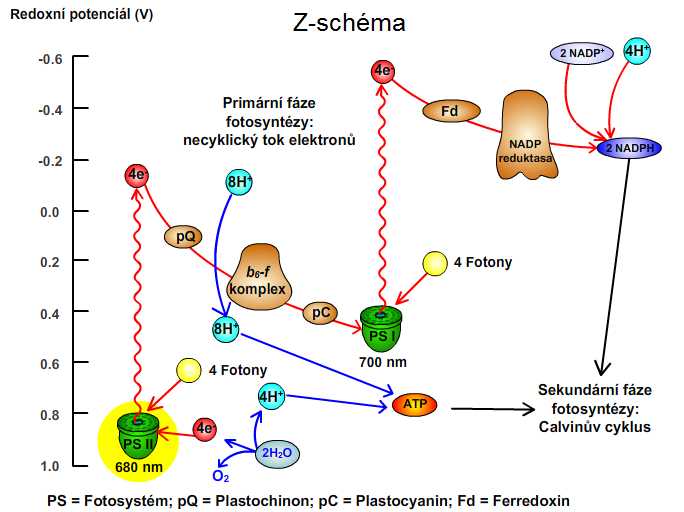
Obr. 14: Schéma redoxních potenciálů. Viz též animace / video / youtube: https://youtu.be/0kRDE7er0Qw.
2.7. Cyklický tok elektronů
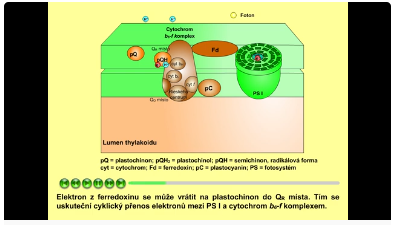
Elektron z ferredoxinu se může vrátit na plastochinon do QR místa. Tím se uskuteční cyklický přenos elektronů mezi PS I a cytochrom b6-f komplexem. Cyklický tok elektronů má za následek zvýšení protonového gradientu, což může vést k vyšší tvorbě ATP. NADPH při cyklickém toku nevzniká, neboť elektrony, které jsou nutné k redukci NADP+ na NADPH, se vracejí zpět na cytochrom b6-f komplex.
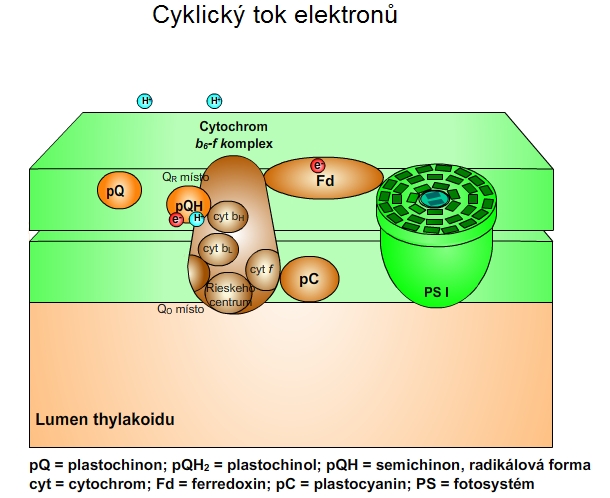
Obr. 15: Cyklický tok elklektronů. Viz též animace / video / youtube: https://youtu.be/i3WeOw-6ziE.
3. Sekundární fáze fotosyntézy
3.1. K čemu dochází v Calvinově cyklu a kde reakce Calvinova cyklu probíhají?
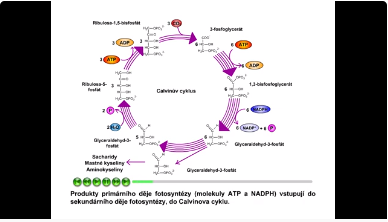
Produkty primárního děje fotosyntézy (molekuly ATP a NADPH) vstupují do sekundárního děje fotosyntézy, do tzv. Calvinova cyklu. NADPH zde působí jako redukční činidlo, ATP jako makroergická sloučenina, která svým rozkladem dodává energii endergonickým procesům. V Calvinově cyklu se anorganický uhlík (vázaný v molekule oxidu uhličitého) mění na uhlík organický. Akceptorem oxidu uhličitého je ribulosa-1,5-bisfosfát, enzym katalyzující tuto reakci se nazývá ribulosabisfosfátkarboxylasa (RuBisCO). V Calvinově cyklu vzniká glyceraldehyd-3-fosfát, který se metabolickými drahami přeměňuje na sacharidy a jiné organické látky.
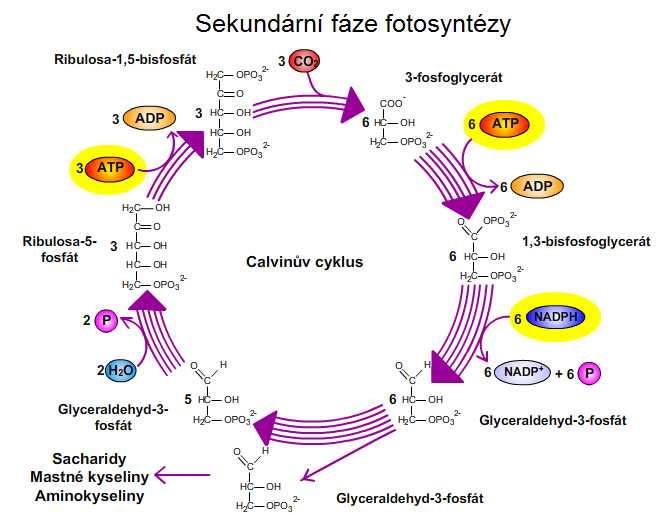
Obr. 16: Calvinův cyklus. Viz též animace / video / youtube: https://youtu.be/JD_7QeQErbc.
Model enzymu Rubisco:
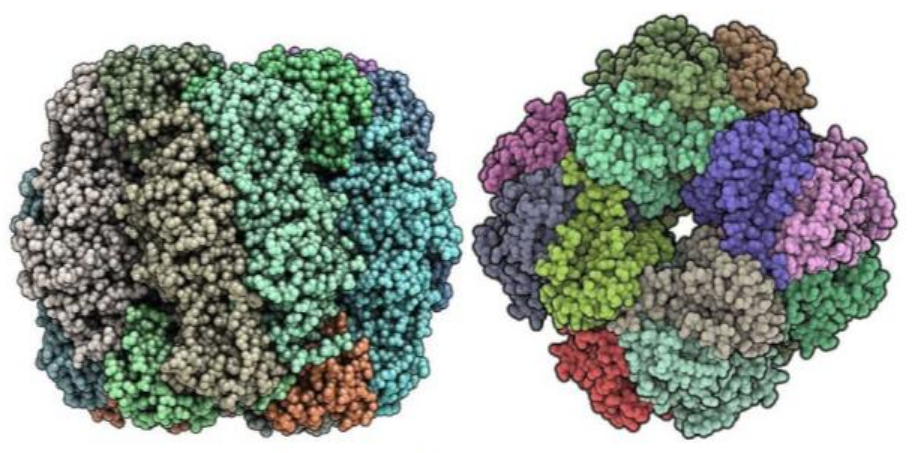
Obr. 17: Struktura enzymu RuBisCO (pohled z dvou různých úhlů). Enzym je složen celkem z 16 podjednotek (polypeptidových řetězců), které jsou na obrázku barevně vyznačené. Autor doc. RNDr. Václav Martínek, Ph.D.
3.2. Fotorespirace a C4 rostliny
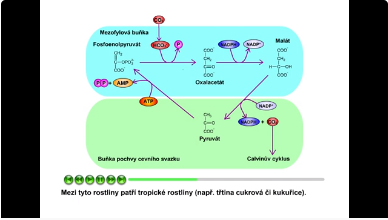
Rostliny nemusí kyslík pouze produkovat, ale mohou ho (vedle mitochondriálního dýchání) vázat místo CO2. Jedná se o tzv. fotorespiraci, která omezuje rychlost rostlin. Některé druhy rostlin koncentrují CO2 ve fotosyntetizujících buňkách, čímž se omezí ztráty vzniklé fotorespirací. Jedná se o tzv. C4 rostliny. Mezi tyto rostliny patří tropické rostliny (např. třtina cukrová či kukuřice). C4-rostliny obsahují 2 typy buněk: mezofylové buňky (fixace CO2) a buňky pochvy cévního svazku (uvolnění CO2 do Calvinova cyklu). V chloroplastech mezofylových buněk chybí Rubisco. Tyto buňky přeměňují CO2 na HCO3-, který reaguje s fosfoenolpyruvátem za vzniku oxalacetátu. Oxalacetát je redukován na malát, který přechází do buněk cevního svazku, kde se dekarboxyluje na pyruvát. Vzniklý CO2 vstupuje do Calvinova cyklu. Oxalacetát a malát jsou čtyřuhlíkaté kyseliny, proto označení C4 rostliny. Fotosyntéza u C4 rostlin je energeticky více náročná než u C3 rostlin, avšak tímto mechanismem úplně potlačí fotorespiraci.
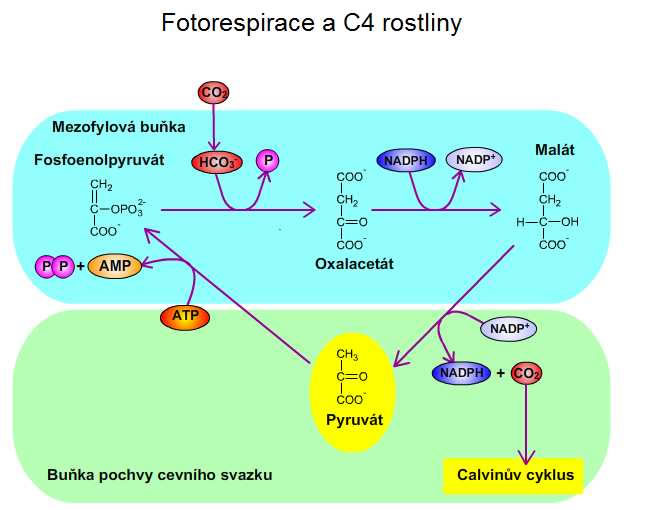
Obr. 14: C4 rostliny. Viz též animace / video / youtube: https://youtu.be/LOxqFU97JUw.
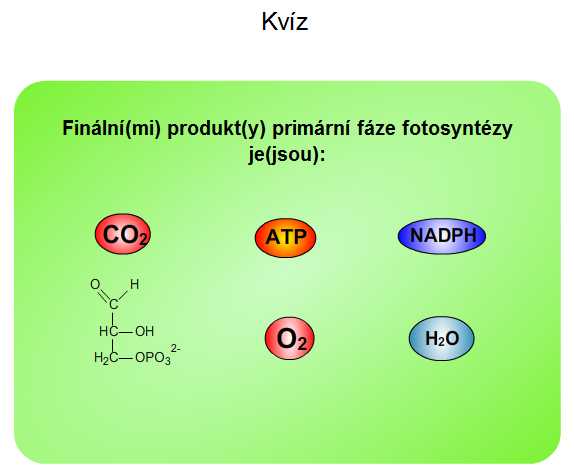
4. Kvíz - fotosyntéza
Obr. 15: Kvíz: video / https://youtu.be/WiXxFEbhSpM
5. Seznam zkratek
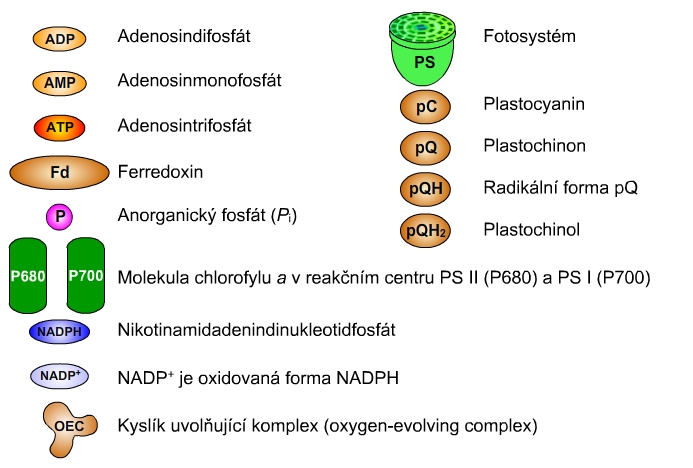
Obr. 15: Seznam zkratek.
6. Použitá literatura
-
Alberts, B.; Bray, D.; Hopkin, K.; Johnson, A.; Lewis, N.; Raff, M.; Roberts, K.; Walter, P. Essential Cell Biology: An Introduction to Molecular Biology of the Cell; Garland Publishing, Inc.: New York, 1998; pp 840−855.
-
Raghavendra, A. S. Photosynthesis: A Comprehensive Treatise; Cambridge University Press: United Kingdom, 2000; pp 87−104.
-
Heldt, H. W.; Piechulla, B. Plant Biochemistry, 4th ed.; Elsevier: United States of America, 2011; pp 65−109.
-
Voet, D. J.; Voet, J. G. Biochemistry, 4th ed.; John Wiley & Sons, Inc.: United States of America, 2011; pp 901−939.